Hiermit bestätige ich, dass ich einen medizinischen oder pharmazeutischen Beruf ausübe [Ärzt*in, Apotheker*in, Pharmazeutisch-technische*r Assistent*in (PTA), Medizinische*r Fachangestellte*r (MFA)].
BadgesNeurologie
Kognitive Störungen

Herausgeber*innen
Hans-Christoph Diener, Helmuth Steinmetz, Oliver Kastrup
Autor*innen
Kathrin Reetz
Letzte Änderung
22.02.2026
Quelle
Reetz K. Kognitive Störungen. In Diener H, Steinmetz H, Kastrup O, Hrsg. Referenz Neurologie. 1. Auflage. Stuttgart: Thieme; 2019, Aktualisierung vom 22.02.2026.
Steckbrief
Kognitive Störungen können unterschiedliche kognitive Domänen umfassen, z.B. das Gedächtnis, die Auffassung und Rechnen, Orientierung, Denken, Sprache und Sprechen, die Lernfähigkeit, Urteilsvermögen und Entscheidungsfähigkeit. Es werden unterschiedliche Schweregrade von der leichten kognitiven Störung bis hin zur leichten, mittelschweren und schweren Demenz unterschieden. Kognitive Störungen können ganz unterschiedliche Ursachen haben, die häufigste erworbene Ursache im Alter ist die Alzheimer Krankheit; es existieren aber viele weitere neurodegenerative, neuropsychiatrische, internistische und toxische Ursachen. Daher sollte die Ursachenabklärung inkl. Risikofaktoren im Vordergrund stehen, um eine entsprechende Behandlung einleiten zu können.
Definition
- Die kognitive Störung ist ein Oberbegriff und Syndrom. Kognitive Störungen bezeichnen eine oder mehrere kognitive Funktionseinschränkungen, die z.B. das Gedächtnis, die Auffassung und Rechnen, Orientierung, Denken, Sprache und Sprechen, die Lernfähigkeit, Urteilsvermögen und Entscheidungsfähigkeit umfassen können. Kognitive Störungen können ganz unterschiedliche Ursachen haben, die häufigste Ursache im Alter ist die Alzheimer-Krankheit.
- Kognitive Störungen sind das Kernsymptom der leichten kognitiven Störung (mild cognitive impairment, MCI) und der Demenz.
- Die leichte kognitive Störung (leichte neurokognitive Störung, engl. mild kognitive impairment [MCI]) ist syndromal über das Vorliegen objektiver kognitiver Beeinträchtigungen definiert, die eine Verschlechterung von einem unbeeinträchtigten Ausgangsstadium darstellen, aber nicht so stark ausgeprägt sind, dass sie die selbstständige Lebensführung beeinträchtigen [1]. Bei der Demenz hingegen ist die Alltagskompetenz nicht mehr uneingeschränkt gegeben.
- Nach der ICD-10-GM-Definition ist Demenz (F00-F03) ist ein Syndrom als Folge einer meist chronischen oder fortschreitenden Krankheit des Gehirns mit Störung vieler höherer kortikaler Funktionen, einschließlich Gedächtnis, Denken, Orientierung, Auffassung, Rechnen, Lernfähigkeit, Sprache und Urteilsvermögen. Das Bewusstsein ist nicht getrübt. Die kognitiven Beeinträchtigungen werden gewöhnlich von Veränderungen der emotionalen Kontrolle, des Sozialverhaltens oder der Motivation begleitet, gelegentlich treten diese auch eher auf. Dieses Syndrom kommt bei Alzheimer-Krankheit, bei zerebrovaskulären Störungen und bei anderen Zustandsbildern vor, die primär oder sekundär das Gehirn betreffen.
Epidemiologie
Häufigkeit
- In der epidemiologischen Betrachtung kognitiver Störungen ist insbesondere die Epidemiologie der Demenzerkrankungen von Bedeutung. Derzeit leben weltweit mehr als 55 Millionen Menschen mit Demenz, und es treten jedes Jahr fast 10 Millionen neue Fälle auf [2]. In Deutschland sind etwa 1,8 Millionen Menschen von Demenz betroffen, und es kommen jährlich etwa 440.000 neue Erkrankungen hinzu. Demenz ist derzeit die siebthäufigste Todesursache weltweit und eine Hauptursache für Behinderungen und Pflegebedürftigkeit bei älteren Menschen.
- Es gibt verschiedene Formen von kognitiven Störungen und Demenz. Die Alzheimer-Krankheit ist die häufigste Form und macht 60-70% der Fälle aus. Weitere wichtige Formen sind die vaskuläre Demenz (ca. 16%), die Demenz mit Lewy-Körperchen (ca. 5-8%) und eine Gruppe von Krankheiten, die zur frontotemporalen Demenz beitragen (eine Degeneration des Frontal- und Temporallappens des Gehirns). Demenz kann auch nach einem Schlaganfall (vaskuläre Demenz) auftreten oder im Zusammenhang mit bestimmten Infektionen wie HIV, schädlichem Alkoholkonsum, wiederholten körperlichen Verletzungen des Gehirns (chronisch-traumatische Enzephalopathie) oder aufgrund von Ernährungsmängeln.
Altersgipfel
- Demenzerkrankungen nehmen mit steigendem Alter exponentiell zu. Während im Alter von unter 65 Jahren etwa 0,1 % der Bevölkerung von einer Demenz betroffen ist, steigt dieser Wert auf etwa 13 % bis 16 % im Alter von 80 bis 84 Jahren [1]. Im Alter von 100 Jahren und darüber sind 49 % bis 58 % an einer Demenz erkrankt.
Geschlechtsverteilung
- Im Hinblick auf die Gesamtprävalenz sind Frauen in jedem Alter häufiger betroffen als Männer. Bei der Alzheimer-Krankheit war bei Personen im Alter von 60 bis 69 Jahren die Prävalenz bei Frauen 1,9-mal höher als bei Männern, während die Prävalenz einer vaskulären Demenz bei Männern 1,8-mal höher war als bei Frauen [3].
Prädisponierende Faktoren
- Das Vorliegen eines Risikofaktors erhöht die Wahrscheinlichkeit für das Auftreten einer Krankheit, in diesem Fall einer Demenz. Wir unterscheiden beeinflussbare und nicht beeinflussbare Risikofaktoren [4], [5].
- Beeinflussbare Risikofaktoren
- Im frühen Lebensalter:
- geringe Bildung (etwa 5 Prozent)
- Im mittleren Lebensalter:
- unbehandelte Hörminderung (etwa 7 Prozent)
- hohes LDL-Cholesterin (etwa 7 Prozent)
- Depression (etwa 3 Prozent)
- Hirnverletzungen (etwa 3 Prozent)
- Bewegungsmangel (etwa 2 Prozent)
- Diabetes mellitus (etwa 2 Prozent)
- Rauchen (etwa 2 Prozent)
- Bluthochdruck (etwa 2 Prozent)
- Übergewicht (etwa 1 Prozent)
- erhöhter Alkoholkonsum (etwa 1 Prozent)
- Im hohen Lebensalter:
- soziale Isolation (etwa 5 Prozent)
- Luftverschmutzung (etwa 3 Prozent)
- Sehminderung (etwa 2 Prozent)
- Im frühen Lebensalter:
- Nicht beeinflussbare Risikofaktoren
- Alter
- Geschlecht
- Genetik
- Apolipoprotein-E
- familiäre Anamnese
- Es ist von großer Bedeutung, zwischen beeinflussbaren und nicht beeinflussbaren Risikofaktoren zu unterscheiden. Das Alter gilt als nicht-beeinflussbarer Hauptrisikofaktor für kognitive Störungen und Demenzerkrankungen. Bei den beeinflussbaren Risikofaktoren gibt es zahlreiche Maßnahmen, die ergriffen werden können. Regelmäßige Arztbesuche und eine entsprechende medizinische Behandlung ermöglichen die Kontrolle bestimmter Risikoerkrankungen wie Bluthochdruck oder Diabetes. Zudem können Veränderungen im Lebensstil, wie vermehrte körperliche Aktivität und eine ausgewogene Ernährung (beispielsweise nach dem mediterranen Vorbild), Übergewicht reduzieren. Soziales Engagement kann der sozialen Isolation entgegenwirken, und das Tragen eines Hörgeräts bei bestehender Hörminderung trägt ebenfalls dazu bei, viele beeinflussbare Risikofaktoren für das Auftreten von Demenz zu minimieren. Des Weiteren zeigen Studien, dass auch der regelmäßige und ausreichende Schlaf (7-8 Stunden pro Nacht) eine wichtige Rolle in der Erholung und Regeneration des Gehirns einnimmt, und bei Schlafstörungen das Risiko einer Demenz steigt.
Ätiologie und Pathogenese
- Die Ätiologie und Pathogenese der kognitiven Störung sind vielfältig. Die häufigste Ursache für eine kognitive Störung im Alter ist die Alzheimer-Krankheit (s. Kap. Alzheimer-Krankheit). Neben der Alzheimer-Krankheit, der Demenz mit Lewy-Körpern, der frontotemporalen Degeneration und der vaskulären kognitiven Störung kann eine kognitive Störung auch bei zahlreichen anderen Erkrankungen auftreten. Dies können degenerative Bewegungsstörungen, namentlich die Parkinson-Krankheit, die progressive supranukleäre Paralyse, die kortikobasale Degeneration oder die Huntington-Krankheit sein. Sie kann aber auch in Verbindung mit Infektionen, Stoffwechselstörungen, eine Depression oder einen anderen psychischen oder Verhaltensstörungen auftreten.
Klassifikation und Risikostratifizierung
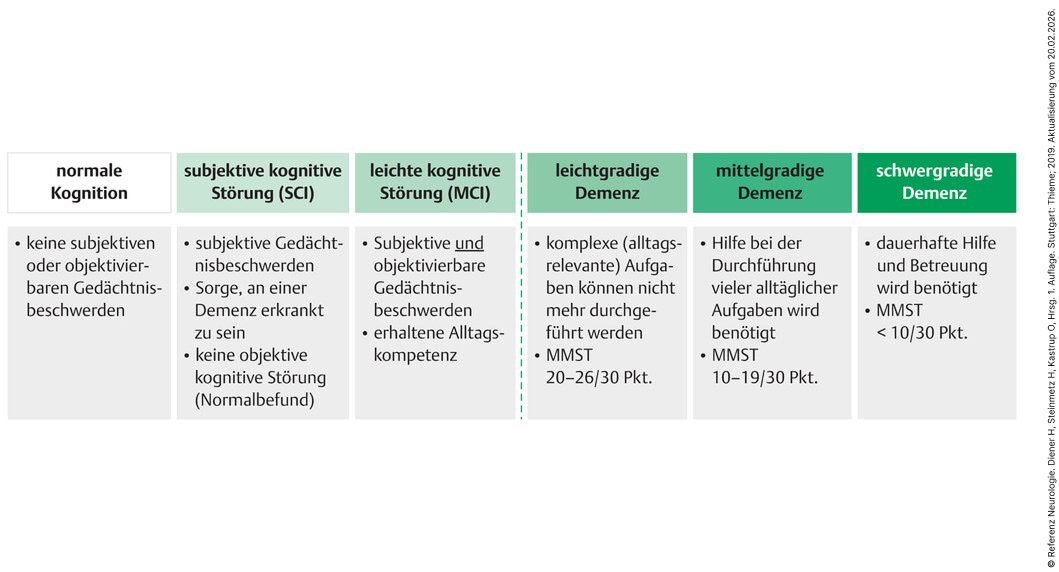
- Kognitive Störungen und Demenzen können auf Syndromebene hinsichtlich des Schweregrades eingeteilt werden (Abb. 00.1_Akt3). Das Spektrum reicht von einer normalen kognitiven Leistung, einer subjektiven kognitiven Störung (kognitive Störung nicht objektivierbar), einer leichten kognitiven Störung (ohne Alltagsrelevanz) bis hin zu einer Einschränkung alltagsrelevanter Aufgaben als klinisch manifestes Stadium einer Demenz, die je nach Schweregrad in leicht, moderat und schwer eingeteilt werden kann.
Abb. 00.1_Akt3 Einteilung der kognitiven Störungen und Demenzen auf Syndrom-Ebene.
Symptomatik
- Die Kernsymptomatik umfasst kognitive Störungen sämtlicher Art. In der Neuropsychologie werden verschiedene kognitive Domänen untersucht.
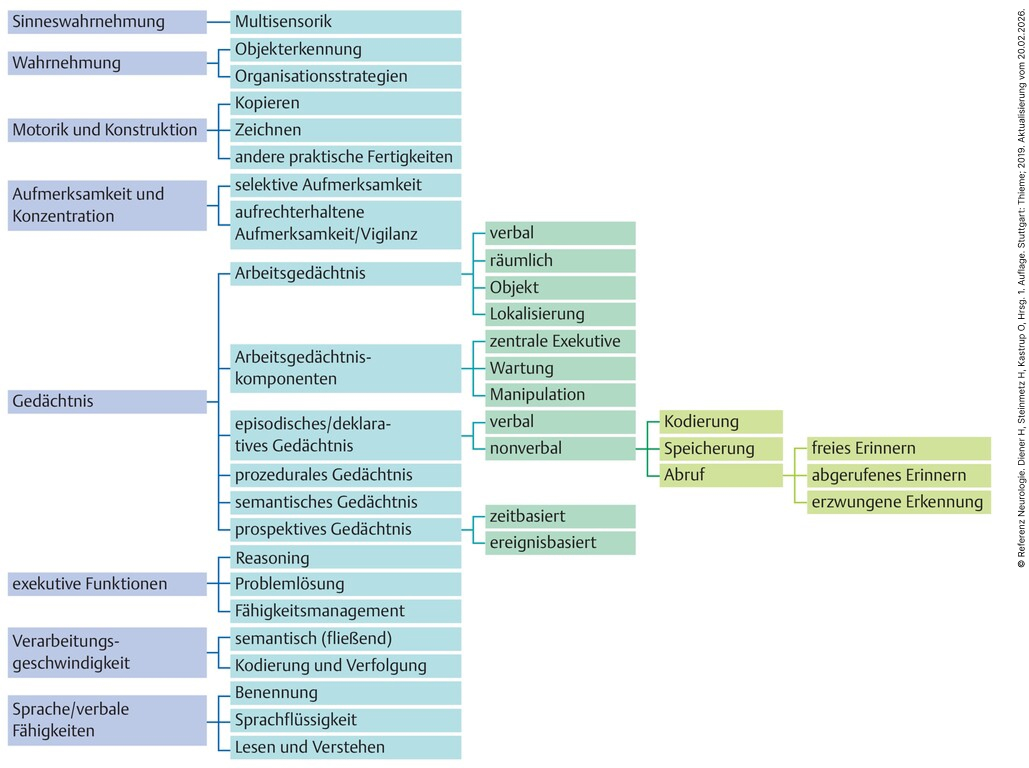
- In der Neuropsychologie wird die kognitive Leistung in der Regel in Form von Funktionsbereichen konzeptualisiert (Abb. 00.2_Akt3). Diese Bereiche sind hierarchisch aufgebaut, wobei sich der unterste Bereich auf grundlegendere sensorische und wahrnehmungsbezogene Prozesse und der oberste Bereich auf Elemente der exekutiven Funktion und der kognitiven Kontrolle bezieht. Die Bereiche sind nicht unabhängig voneinander, und die exekutive Funktion übt die Kontrolle über die Nutzung grundlegenderer Prozesse aus. Beurteilungen sind in der Regel auf Teilbereiche jedes Fähigkeitsbereichs ausgerichtet, und eine sorgfältige Kombination von Aufgaben kann Leistungsmuster aufzeigen, die mit einer Vielzahl verschiedener neurologischer und neuropsychiatrischer Erkrankungen übereinstimmen.
Abb. 00.2_Akt 3 Funktionsbereiche der kognitiven Leistung [6].
Diagnostik
Diagnostisches Vorgehen
-
Zur Diagnostik gehören eine (Fremd-)Anamnese, eine kognitive Testung sowie eine neurologische, internistische und psychopathologische Untersuchung. Die weiterführende Diagnostik bei V.a. auf eine neurodegenerative Erkrankung beinhaltet zusätzlich noch eine Laboruntersuchung, Bildgebung und Liquordiagnostik.
Anamnese
-
Eine genaue Erhebung der Eigen-, Fremd-, Familien- und Sozialanamnese unter Einschluss der vegetativen und Medikamentenanamnese im Hinblick auf besondere Problembereiche, Alltagsbewältigung und den bisherigen Verlauf sind für eine ätiologische Zuordnung und Schweregradeinteilung wichtig.
Körperliche Untersuchung
-
Es ist unerlässlich, eine internistische, neurologische und psychopathologische Untersuchung durchzuführen, da eine Reihe von Krankheiten zu neurokognitiven Störungen führen können. Es ist dabei besonders wichtig, auf kardiovaskuläre, metabolische und endokrinologische Krankheiten, Parkinson-Symptome, Depressionen und andere psychische oder Verhaltenssymptome zu achten, da diese Anzeichen für die zugrunde liegende Krankheit sein können. Bei einer neurologischen Untersuchungen sollte ein besonderes Augenmerk auf das Vorliegen von Parkinson-Symptomen z.B. Rigor, Tremor, Bradykinese oder eine posturale Instabilität, aber auch anderen Bewegungsstörungen wie Hyperkinesien oder Dystonien gelegt werden. Es gibt verschiedene validierte Skalen zur Beurteilung von psychischen und Verhaltensstörungen, die mit Demenz in Verbindung stehen.
Psychometrische Untersuchung
Kognitive Untersuchung
- Zur orientierenden Einschätzung von kognitiven Störungen und der Schweregradeinteilung werden Screeningverfahren eingesetzt, z.B. der Mini-Mental-Status-Test (MMST) und der Montreal Cognitive Assessment Test (MoCA). Der MMST ist ein immer noch weit verbreitete Test, bestehend aus 10 Bereichen, in den Aufmerksamkeit, Sprache und visuomotorische Funktionen überprüft werden. Die maximal erreichbare Gesamtpunktzahl beträgt 30 Punkte.
- Orientierende Demenz-Schweregradeinteilung anhand des MMST:
- leicht: 20 bis 26 Punkte
- mittelschwer: 10 bis 19 Punkte
- schwer: 0 bis 9 Punkte
- Der Kurztest MoCA-Test, der in etwa 10 Minuten abgeschlossen werden kann, bewertet verschiedene kognitive Bereiche wie Kurzzeit- und Arbeitsgedächtnis, Merkfähigkeit, Wortflüssigkeit, Abstraktionsvermögen, Exekutive Funktionen, Visuokonstruktion, Aufmerksamkeit und Orientierung. Die Testergebnisse reichen von 0 bis 30 Punkten, wobei das Bildungsniveau des Probanden in die Auswertung einbezogen wird. Im Vergleich zum MMST ist der MoCA sensitiver für leichte kognitive Beeinträchtigungen und eignet sich gut zur Verfolgung von Krankheitsverläufen aufgrund seiner Alternativversionen, die wichtig sind, um Lerneffekte zu minimieren, zu wiederholten Untersuchungen. Der MoCA ist zudem in vielen verschiedenen Sprachen verfügbar.
- Für die ausführlichere Diagnostik und Differenzialdiagnostik sind weitere standardisierte neuropsychologische Testverfahren und diagnostische Interviews entwickelt worden. Zu diesen gehört u. a. die neuropsychologische Testbatterie
- CERAD-Plus, die im deutschsprachigen Raum weit verbreitet ist. Andere standardisierte Testbatterien sind etwa die „Alzheimer’s Disease Assessment Scale-cognitive Subscale“ (ADAS-cog) und „Clinical Dementia Rating Scale“ (CDR). Sie erfassen u. a. die kognitiven Bereiche Lernen und Gedächtnis, Exekutivfunktionen, Objekt- und Raumkognition, Aufmerksamkeit, Praxis, Sprache und Handlungsplanung. Die dadurch gewonnenen neuropsychologischen Störungsprofile können klinisch dabei helfen, erste Hypothesen zur Ursache zu bilden.
- Wann ist eine ausführliche neuropsychologische Untersuchung sinnvoll? Bei Verdacht auf eine leichte kognitive Störung oder leichtgradige Demenz sollte eine neuropsychologische Untersuchung ergänzt werden, da die neuropsychologischen Defizitprofile typische Charakteristika je nach der zugrundeliegenden Ursache aufweisen können. Typisch für eine Alzheimer-Krankheit sind beispielsweise Defizite vor allem in den kognitiven Domänen Lernen, Gedächtnis und Visuokonstruktion. Neuropsychologische Profile sind im Frühstadium am aussagekräftigsten. Wenn die Demenz vom Früh- zum Spätstadium fortschreitet, werden die Grenzen zwischen den einzelnen Formen immer unschärfer. Ab dem mittelschweren Demenzstadium reicht häufig ein Screenintest zur Bestimmung des Schweregrades aus.
Funktionsskalen
- Die Alltagskompetenz einer Person und ihre Fähigkeit sich selbst zu versorgen, hängen zwar eng mit der kognitiven Leistung zusammen, werden aber auch von anderen Faktoren beeinflusst, zum Beispiel Hörvermögen, Sehkraft, motorische Funktion. Daher erlaubt das Abschneiden in kognitiven Tests keine uneingeschränkten Rückschlüsse auf die Bewältigung des Alltags (Activities of Daily Living, ADL). Diese Fähigkeit wird vielmehr mit den sogenannten Funktions-oder Beurteilungsskalen bewertet, von denen einige in übergeordneten Demenzskalen und Stadieneinteilungen enthalten sind. Zum Teil werden basale Funktionen der Selbstständigkeit wie Anziehen, Essen und Gehen erfasst, zum Teil aber auch komplexere Alltagsaktivitäten wie telefonieren, einkaufen oder mit Geld umgehen.
- Die Bayer Activities of Daily Living Scale (B-ADL) dient beispielsweise als Screening-Tool für Demenzerkrankungen und zur Bewertung von Alltagskompetenzbeeinträchtigungen bei älteren Patienten, die kognitive Leistungseinbußen aufweisen. Dies geschieht durch ein Verfahren der Fremdbeurteilung, das von einer primären Bezugsperson oder Betreuer durchgeführt wird. Der Test besteht aus 25 Items, die Alltagsprobleme darstellen und auf einer 10-stufigen Ratingskala bewertet werden. Durch die Bereitstellung von Durchschnittswerten und Standardabweichungen für verschiedene Schweregrade kann eine Normierung erfolgen. Die Bearbeitungszeit beträgt etwa 10 bis 15 Minuten.
Verhaltensskalen
- Behaviorale Symptome sind Veränderungen des Erlebens und Verhaltens. So können Wahn, Halluzinationen, Depression, Apathie oder Unruhe einen wesentlichen Bestandteil des Demenzsyndroms darstellen. Psychische und Verhaltenssymptome sind häufig bei Demenz und leichter kognitiver Störung. Eine Erfassung mithilfe geeigneter Instrumente kann bei der Befundinterpretation und Diagnostik neuropsychologischer Untersuchungen hilfreich sein. Außerdem leiten sich hieraus eventuell therapeutische Maßnahmen ab.
- Die Geriatrische Depressionsskala (GDS) ist ein weltweit anerkanntes Bewertungsinstrument, das durch einen vom Patienten zu beantwortenden Fragebogen Anzeichen für mögliche Altersdepression oder depressive Stimmung ermitteln kann. Der Fragebogen besteht normalerweise aus 15 Fragen und ist geeignet für gesunde ältere Menschen, medizinisch erkrankte Personen und solche mit leichter bis mäßiger kognitiver Beeinträchtigung.
- Das Neuropsychiatrische Inventar (NPI) wurde entwickelt, um die neuropsychiatrischen Symptome und die Psychopathologie von Patienten mit der Alzheimer-Krankheit und anderen neurodegenerativen Erkrankungen zu beurteilen. Der NPI umfasst zehn verhaltensbezogene und zwei neurovegetative Bereiche: Wahnvorstellungen, Halluzinationen, Erregung/Aggression, Depression/Dysphorie, Angst, Hochstimmung/Euphorie, Apathie/Indifferenz, Enthemmung, Reizbarkeit/Labilität, abweichendes motorisches Verhalten, Schlaf- und nächtliche Verhaltensstörungen, Appetit- und Ess-Störungen.
Labor
Blutdiagnostik
- Im Rahmen der Basisdiagnostik werden folgende Blutuntersuchungen empfohlen: Blutbild, Elektrolyte (Na+, K+, Ca2+), Nüchtern-Blutzucker, TSH, Blutsenkung oder CRP, GOT, γ-GT, Kreatinin, Harnstoff, Vitamin B12, eGFR [1].
- Dies kann beim Verdacht auf spezifische Erkrankungen erweitert werden.
- Bei klinisch unklaren Situationen, wie z.B. atypischen Symptomen, jungem Manifestationsalter oder schneller Krankheitsprogression, oder bei spezifischen klinischen Verdachtsdiagnosen, sind gezielte erweiterte Laboruntersuchungen durchzuführen. Dazu gehören unter anderem: Differenzial-Blutbild, Blutgasanalyse (BGA), Drogentests, Urinanalysen, Lues- und HIV-Serologie, Messungen der Konzentrationen von Phosphat, HBA1c, Homocystein, fT3, fT4, Schilddrüsen-Antikörper, Kortisol, Parathormon, Coeruloplasmin, Vitamin B6, Borrelien-Serologie, Blei, Quecksilber, Kupfer und Folsäure.
- In naher Zukunft werden auch Messungen der Neurodegenerationsmarker im Blut verfügbar sein.
Liquordiagnostik
- Die Liquordiagnostik dient der Diagnose oder dem Ausschluss neurodegenerativer Erkrankungen, insbesondere der Alzheimer-Krankheit, aber auch anderer Erkrankungen (z. B. entzündlicher ZNS-Erkrankungen). Im Liquor sind Korrelate der neuropathologischen Veränderungen, die die Alzheimer-Krankheit definieren, messbar. Die diesbezüglich relevanten Parameter, die immer gemeinsam untersucht werden sollten, sind die Beta-Amyloide Aβ(1-42) und Aβ(1-40), die Amyloid-Ratio (das Verhältnis von Aβ[1-42]/Aβ[1-40]), das Gesamt-Tau (ggf. auch Neurofilament [NfL]) und das Phospho-Tau (pTau).
Bildgebende Diagnostik
MRT
- Eine weitere wichtige Untersuchung ist die strukturelle Bildgebung, optimalerweise mithilfe von Magnetresonanztomografie (MRT), um mögliche strukturelle Abnormalitäten wie eine Hirnvolumenminderung in bestimmten Gehirnarealen – eine sogenannte Atrophie – oder auch vaskuläre Veränderungen zu detektieren.
PET/PET-CT
-
Zur weiteren Differenzialdiagnostik existieren auch weitere Bildgebungsmethoden, z. B. die Positronen-Emissions-Tomografie (PET), bspw. mit dem [18F]-Fluo-rodeoxyglucose (FDG)-PET, oder die Dopamintransporter-Szintigraphie (DaTSCAN) bei Verdacht auf eine Parkinson-Krankheit. Die zerebrale „Amyloid-PET“ und „Tau-PET“ werden derzeit vorwiegend in der Forschung und in klinischen Studien eingesetzt, können aber bei schwierigen Fällen differenzialdiagnostisch zur Klärung beitragen, insbesondere wenn im Rahmen der Differenzialdiagnostik einer Alzheimer-Demenz keine Lumbalpunktion durchgeführt werden kann.
Histologie, Zytologie und klinische Pathologie
Liquordiagnostik
- Der Aspekt Liquordiagnostik wird im Rahmen einer Labormethode weiter oben im Modul behandelt.
Differenzialdiagnosen
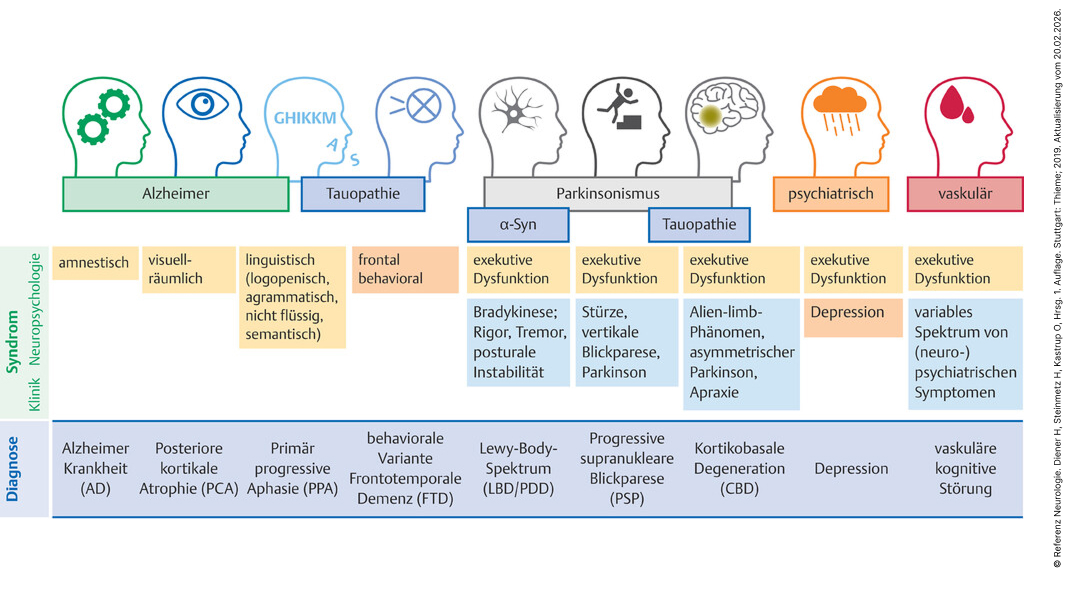
- Je nach Ursache sind spezifische kognitive Domänen betroffen, die neuropsychologischen Defizitprofile helfen in der Zusammenschau mit dem klinischen Bild und der Zusatzdiagnostik bei der Diagnosestellung, damit dann die entsprechende Therapie eingeleitet werden kann. Abb. 00.3_Akt3 zeigt eine Übersicht über häufige neurodegenerative aber auch psychiatrische und vaskuläre Differentialdiagnosen.
- Die kognitiven Kernsymptome der Alzheimer-Krankheit im frühen Krankheitsstadium ist primär die Gedächtnisstörung (amnestische kognitive Störung) aber auch Störungen des visuell-räumlichen Denkens und des Benennens.
- Im späteren Verlauf entwickelt sich eine kortikale Demenz mit ausgeprägten Neu- und Altgedächtnisstörungen, visuell-räumlicher Verarbeitungsstörung, Apraxie, Agnosie und einer Sprachstörung s. Kap. zur Alzheimer-Krankheit.
- Zu den atypischen häufigen Alzheimer Varianten zählen die posteriore kortikale Atrophie (PCA), die typischerweise mit langsam progredienten visuellen Störungen beginnt und die logopenische primär progressive Aphasie (lvPPA), bei der zu Beginn eine langsam fortschreitende Sprachstörung im Vordergrund steht. Bei der frontotemporalen Demenz (FTD) unterscheiden wir eine primär progressive Aphasie (PPA), die logopenischer, nicht-flüssiger agrammatischer oder semantischer Natur sein kann oder eine behaviorale Variante (bvFTD), die zunächst dominiert von Verhaltensveränderungen ist, sich aber häufig auch exekutive Störungen finden. Finden sich kognitive Störungen, insbesondere exekutive Dysfunktionen, zusammen mit einem Parkinson-Symptomen muss an eine Parkinson-Krankheit (PD) mit leichter kognitiver Störung (PD-MCI) oder Demenz (PDD), aber wenn auch seltener vorkommend an eine Lew-Body-Demenz (LBD), eine progressive supranukleäre Blickparese (PSP) oder eine kortikobasale Degeneration gedacht werden (s. Kap. Parkinson-Syndrome). Exekutive Störungen können aber auch einen Hinweis auf eine zugrundeliegende Depression oder vaskulärer Genese sein (s. Kap. Vaskuläre Demenzen). Gerade im Hinblick auf die Differentialdiagnosen zeigt sich wie wichtig der klinische Gesamteindruck ist, denn das Erkennen von klinischen Symptomen wie zum Beispiel Bradykinese, Rigor und Tremor kann wichtige Rückschlüsse auf die Ursache kognitiver Störungen geben.
Abb. 00.3_Akt3 Schematische Übersicht der Differenzialdiagnosen kognitiver Störungen.
Therapie
- Die Therapie richtet sich nach der Ursache, die entsprechend behandelt werden muss.
- Aufgrund der großen Bedeutung der Risikofaktoren, ist eine sorgfältige Identifikation dieser nötig, um auch diese entsprechend behandeln zu können.
Therapeutisches Vorgehen
- Wichtigstes therapeutisches Ziel ist die Verhinderung des Fortschreitens der Erkrankung durch Behandlung der Grundkrankheit bzw. der beeinflussbaren Risikofaktoren.
- Neben einer pharmakologischen Behandlung, sofern sie zur Verfügung steht, existieren auch nicht pharmakologische Therapien von kognitiven, psychischen und Verhaltenssymptomen.
- Dazu gehören psychosoziale Interventionen wie kognitive Verfahren (z.B. kognitive Training, kognitive Stimulation, Reminiszenz-Therapie, Realitätsorientierung und kognitive Rehabilitation), aber auch künstlerische Therapien (z.B. Musiktherapie); und regelmäßige körperliche Aktivierung.
Nachsorge
- Bei Fortbestehen oder Progredienz können kognitive Kurztests und ggf. neuropsychologische Verlaufskontrollen zur Objektivierung und Therapieanpassung indiziert sein.
Verlauf und Prognose
- Während die primär neurodegenerativen kognitiven Störungen (z.B. Alzheimer-Krankheit, frontotemporale Demenz, Parkinson-Demenz, Lewy-Körperchen-Demenz) langsam fortschreitend verlaufen, sind andere Ätiologien wie zum Beispiel vaskuläre Ursachen oder psychiatrischer Genese nicht zwangsläufig progredient.
Prävention
- Die Prävention von kognitivem Abbau und Demenz ist von großer Bedeutung, insbesondere bei älteren Menschen. Denn kognitive Fähigkeiten beeinflussen die Kommunikation, soziale Interaktion, Ernährung, Bewegung und auch die Medikamenteneinnahme. Sie sind daher wichtige Voraussetzungen, um selbstständig und selbstbestimmt zu leben. Die Kognition verändert sich im Laufe des Lebens – und muss daher bis ins hohe Alter gefördert werden. Durch gezielte Maßnahmen kann das Risiko für geistigen Abbau sowie für Demenz gesenkt werden. Daher ist eine frühzeitige und differenzierte Erfassung kognitiver Defizite und deren Risikofaktoren essentiell. Präventive Maßnahmen tragen hier wesentlich zur einer Verbesserung der Lebensqualität bei.
Synonyme
-
neurokognitive Störung
Keywords
- leichte kognitive Störung
- Demenz, Alzheimer-Krankheit
- neurodegenerative Erkrankungen
- vaskuläre kognitive Störung
- Frontotemporale Demenz
- Parkinson-Demenz
- Lew-Body-Demenz
- Depression
Literatur
Wichtige Internetadressen
- S3-Leitlinie Demenzen, Version 4, 8.11.2023: https://register.awmf.org/de/leitlinien/detail/038-013
Quellenangaben
[1] DGN e. V. & DGPPN e. V. S3-Leitlinie Demenzen, Version 4, 8.11.2023, verfügbarunter: https://register.awmf.org/de/leitlinien/detail/038-013, Zugriff am 19.06.2024
[2] Collaborators GBDN. Global, regional, and national burden of neurologicaldisorders, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurol 2019; 18 (5): 459-480
[3] Cao, Qing et al. ‘The Prevalence of Dementia: A Systematic Review and Meta-Analysis’. 1 Jan. 2020: 1157–1166
[4] Livingston G, Huntley J, Sommerlad A, et al. Dementia prevention, intervention,and care: 2020 report of the Lancet Commission. Lancet 2020; 396 (10248): 413-446
[5] Livingston G, Huntley J, Liu KY, et al. Dementia prevention, intervention, andcare: 2024 report of the Lancet standing Commission. Lancet. 2024;404(10452):572-628. doi:10.1016/S0140-6736(24)01296-0
[6] Harvey, P. D. Domains of cognition and their assessment . Dialogues Clin.Neurosci. 21, 227–237 (2019)