Hiermit bestätige ich, dass ich einen medizinischen oder pharmazeutischen Beruf ausübe [Ärzt*in, Apotheker*in, Pharmazeutisch-technische*r Assistent*in (PTA), Medizinische*r Fachangestellte*r (MFA)].
BadgesPsychische Störungen
Leichte kognitive Störung

Herausgeber*innen
Michael Bauer, Andreas Meyer-Lindenberg, Falk Kiefer, Alexandra Philipsen
Autor*innen
Markus Donix, Robert Haußmann
Letzte Änderung
20.02.2026
Quelle
Donix M, Haußmann R. Leichte kognitive Störung. In Bauer M, Meyer-Lindenberg A, Kiefer F, Philipsen A, Hrsg. Referenz Psychische Störungen. 1. Auflage. Stuttgart: Thieme; 2021, Aktualisierung vom 20.02.2026
Steckbrief
Die leichte kognitive Störung (Mild cognitive Impairment, MCI) ist ein Zwischenstadium im (pathologischen) Kontinuum von altersentsprechender Kognition bzw. subjektiver kognitiver Störung (subjective cognitive decline, SCD) und Demenz. Es handelt sich um ein wichtiges Früh- und Risikosyndrom bei Demenzerkrankungen. MCI umfasst subjektive Einbußen und objektivierbare Defizite in mindestens einer kognitiven Domäne, ohne dass die Kriterien für ein Demenzsyndrom erfüllt sind. Insbesondere bestehen keine alltagsrelevanten Beeinträchtigungen. Ätiologie, Symptomatik und testpsychometrische Profile sind heterogen, was erhebliche prognostische Unterschiede bedingt. Neben metabolischen Störungen und psychiatrischen Erkrankungen kommen auch vaskuläre und neurodegenerative Erkrankungen als mögliche Ursache in Betracht. Während das amnestische MCI (Beeinträchtigung im Gedächtnis) mit einem erhöhten Risiko der Konversion zu einer Demenz vom Alzheimer-Typ vergesellschaftet ist, sind nichtamnestische MCI häufiger ein Prodromalstadium anderer Demenzerkrankungen [4]. Etwa 10% der Patienten mit MCI erkranken jährlich an einer Demenz, häufig ist es aber eine zeitstabile oder sogar reversible Entität.
Aktuelles
Mit Zulassung der Anti-Amyloid-Antikörper Lecanemab und Donanemab stehen in Deutschland seit 2025 erstmals verlaufsmodulierende Therapien zur Behandlung der leichten kognitiven Störung (MCI) im Rahmen einer Alzheimerkrankheit (mit Amyloidnachweis) zur Verfügung [11] [12].
Definition
- MCI beschreibt subjektive kognitive Veränderungen oder das Wahrnehmen kognitiver Defizite durch Zugehörige und testpsychometrisch objektivierbare Defizite in einer oder mehreren kognitiven Domänen wie Exekutivfunktion, Sprache, Gedächtnis oder geteilter Aufmerksamkeit bei erhaltener Alltagskompetenz [1], [5].
- Die Testwerte liegen zwischen 1 und 1,5 Standardabweichungen unter der Alters- und Bildungsnorm [1], sind aber keine Absolutwerte, da die kognitiven Veränderungen in Relation zum intellektuellen Ausgangsniveau zu betrachten sind.
- darüber hinaus wird in early MCI (EMCI, Testwerte zwischen 1 bis 1.5 Standardabweichungen unter Alters- und Bildungsnorm) und late MCI (LMCI) unterschieden [13]
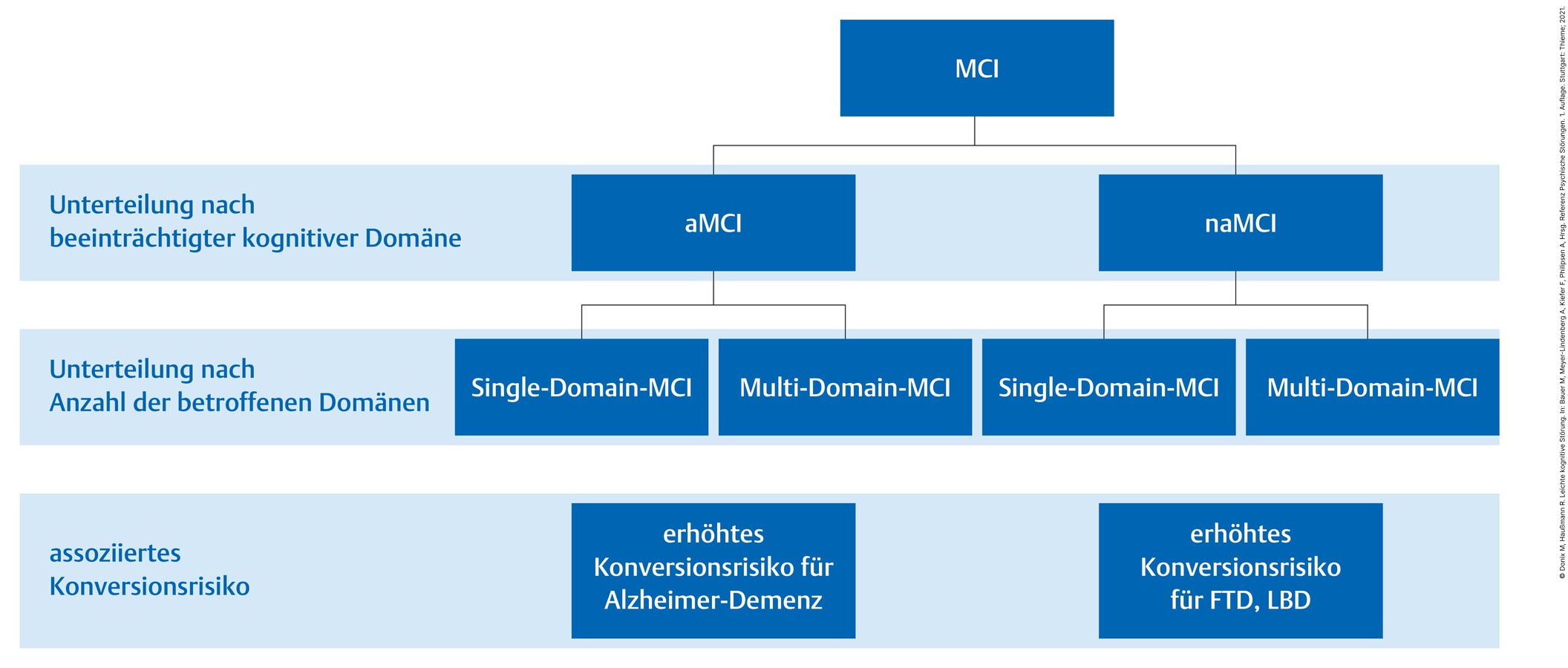
- MCI wird je nach neuropsychologischem Defizitprofil in amnestische und nichtamnestische Formen unterteilt (Abb. 90.1).
- Je nach Anzahl der betroffenen kognitiven Domänen unterscheidet man Single- und Multi-Domain-MCI.
- Die leichte kognitive Störung ist nach ICD-10 und ICD-11 unschärfer definiert als das MCI nach Petersen [5] und kann passagere Leistungsminderungen umfassen, die nicht exakt definiert sind.
- Im DSM-5 wurde die leichte neurokognitive Störung implementiert, die aus klinischer Sicht als äquivalent zum MCI zu betrachten ist. In der ICD-11 beschreibt die „Mild neurocognitive Disorder“ ebenfalls eine nicht die Alltagsfähigkeit einschränkende subjektive kognitive Leistungsminderung, die von testpsychometrisch objektivierbaren Einbußen begleitet wird.
Abb. 90.1 Leichte kognitive Störung (MCI).
Unterteilung des MCI und Konversionsrisiken [5] (aMCI: amnestische MCI, naMCI: nichtamnestische MCI, FTD: frontotemporale Demenz, LBD: Lewy-Körper-Demenz).
Epidemiologie
- Das amnestische MCI ist häufiger als das nichtamnestische MCI (etwa 2:1).
- Allgemeine Konversionsraten zur Demenz sind durch ätiologische Heterogenität variabel (1–25%).
- Die Konversionsrate eines amnestischen MCI zur Demenz beträgt etwa 10–15% pro Jahr
- Die Mehrzahl der MCI ist zeitlich stabil oder sogar reversibel.
- Das Risiko für eine Demenz vom Alzheimer-Typ ist bei Patienten mit MCI im Vergleich zu gleichaltrigen Gesunden etwa 3-fach erhöht [4].
| Merke
|
Häufigkeit
- Die Häufigkeit nimmt mit steigendem Lebensalter zu (65–69 Jahre: 8,4%; 80–84 Jahre: 25,2%) [4].
- Die Inzidenz beträgt bei über 70-Jährigen etwa 5% pro Jahr [6].
Altersgipfel
-
Die Häufigkeit des MCI nimmt mit steigendem Lebensalter zu.
Geschlechtsverteilung
- Nach aktuellem Kenntnisstand existieren keine deutlichen geschlechtsspezifischen Unterschiede hinsichtlich Inzidenz und Prävalenz von MCI insgesamt.
- Aktuelle Befunde lassen eine höhere Prävalenz nichtamnestischer Formen bei Frauen vermuten.
Prädisponierende Faktoren
- Prädisponierende Faktoren sind:
- höheres Lebensalter
- geringe kognitive Reserve und inaktiver Lebensstil
- kardiovaskuläre Risikofaktoren (z.B. Bluthochdruck, Diabetes, Adipositas)
- zerebrovaskuläre Läsionen
- strukturelle Herzerkrankungen
- Vorliegen eines ApoE-4-Allels, nochmals deutlich höheres Risiko bei Homozygoten
Ätiologie und Pathogenese
- Eine Vielzahl von Faktoren kommen einzeln oder in Kombination ätiologisch in Betracht:
- Neurodegeneration (amnestisches MCI: häufig Amyloidpathologie; nichtamnestisches MCI: häufiger Tau-Pathologie, α-Synukleinopathie, TDP-43) mit cholinerger Dysfunktion
- zerebrovaskuläre (zerebrale Mikroangiopathie, cerebrale Amyloidangiopathie) oder gemischte Ätiologien
- psychiatrische Erkrankungen (Depression, bipolar-affektive Störungen, ADHS, PTBS)
- dyskognitive Medikamenteneffekte (bspw. Anticholinerigka, Antihistaminika)
- Schlafstörungen (obstruktives Schlafapnoe-Syndrom, Restless-Legs-Syndrom)
- metabolische Erkrankungen (Vitamin-B12- und Folsäuremangel, Hypothyreose, erheblich schwankende Blutzuckerwerte bei Diabetes mellitus)
- schwere Begleiterkrankungen (Malignome, ausgeprägte Anämie, Herzinsuffizienz, Hypoxie)
- selten andere strukturelle Erkrankungen des Gehirns
- ethyltoxische Genese
- Z. n. Chemotherapie („chemobrain“) [7]
Symptomatik
- Ein MCI ist in Abgrenzung zur subjektiven kognitiven Störung (SCD) testpsychometrisch objektivierbar. Die subjektiv oder durch Zugehörige wahrgenommene Einbuße kann in einer formalen Testung bestätigt, aber auch als Defizit in einer anderen kognitiven Domäne differenziert werden (z. B. Konzentrations- oder Aufmerksamkeitsstörung als Korrelat subjektiver Gedächtnisstörung).
- Die Alltagskompetenz ist nicht beeinträchtigt bzw. subtile Beeinträchtigungen werden gut kompensiert. Die Kriterien für ein Demenzsyndrom sind nicht erfüllt.
- Wenn ein MCI in nur einer Domäne kognitiver Leistungen objektiviert werden kann (Single Domain), spricht man im Falle von Gedächtnisdefiziten von einem amnestischen MCI, andernfalls von nichtamnestischen Formen, da seltener auch Sprache und Exekutivfunktionen relativ isoliert beeinträchtigt sein können. Sind Einbußen in mehreren kognitiven Domänen messbar (Multi Domain), werden Gedächtnisdefizite trotzdem zusätzlich bewertet [5].
- Je nach Ätiologie bestehen variable Beeinträchtigungen der Kritikfähigkeit und Krankheitseinsicht.
- In 25–40% der Fälle besteht eine (oft subklinische) Depressivität.
- Gelegentlich treten andere neuropsychiatrische Symptome auf wie Irritabilität, Ängstlichkeit und Aggressivität.
Diagnostik
- Die Diagnostik sollte gemäß den Leitlinien zur Demenzdiagnostik erfolgen [2].
- Eine „leichte“ Ausprägung kognitiver Einbußen rechtfertigt keine vereinfachte Diagnostik und kann gerade aufgrund der milden Symptomatik besonders differenzierte Untersuchungen erfordern. Ein vorschnelles Attribuieren auf physiologisches Altern sollte nicht erfolgen.
- Die Diagnostik ist relevant für die Detektion reversibler Ursachen, aber auch für die Identifikation geeigneter Patientinnen für die verlaufsmodulierende Therapie mit einem Anti-Amyloid-Antikörper.
- Alle Bestandteile der Diagnostik müssen in der Zusammenschau und im klinischen Kontext bewertet werden, da eine multifaktorielle Genese immer möglich ist. Ebenso müssen nicht alle pathologischen Untersuchungsbefunde für die kognitive Störung ätiologisch relevant sein.
- falls die Ätiologie geklärt werden kann, soll diese der Diagnose hinzugefügt werden [2]
- zu beachten ist, dass gemäß aktueller Leitlinienempfehlungen die Diagnose einer Alzheimer-Krankheit bei typischer Symptomausprägung und eindeutigem Biomarker-Nachweis (Tau- und beta-Amyloid-Pathologie) bereits im Stadium der leichten kognitiven Störung gestellt werden kann [2]
Diagnostisches Vorgehen
- Obligatorische Untersuchungen sind:
- Anamnese, Fremdanamnese und allgemeine körperliche und neurologische Untersuchung sowie psychiatrische Exploration
- Assessment modifizierbarer Risikofaktoren und potentiell dyskognitiv wirksamer Medikamente
- differenzierende neuropsychologische (Verlaufs-)Diagnostik mit validierten Verfahren sowie Depressionsassessment bei klinischem Verdacht [2]
- laborchemische Diagnostik (insbesondere TSH, Vitamin-B12- und Folsäure-Spiegel, ggf. Holotranscobalamin, Methylmalonsäure und Homocystein bei grenzwertigen Vitamin-B12- und Folsäure-Spiegeln)
- zerebrale Bildgebung (vorzugsweise MRT zur Feststellung einer regionalen Atrophie und vaskulärer Läsionen)
- Ergänzende Untersuchungen können sein:
- Liquordiagnostik (Demenz- und Neurodegenerationsmarker)
- Positronenemissionstomografie (FDG-PET, Amyloid-PET wenn Effekt auf klinisches Management zu erwarten) [2]
- Elektroenzephalografie
- ggf. MIBG-Szintigrafie und DaT-SPECT-Untersuchung bei V. a. LBD
- ggf. genetische Diagnostik (CAVE: ApoE-Genotypisierung gemäß aktueller S3-Leitlinie im Rahmen der Diagnostik nicht empfohlen, aber: vor Anti-Amyloid-Antikörpertherapie obligatorisch zur Abschätzung des ARIA-Risikos) [2]
Anamnese
- Bei der Erhebung der Anamnese werden subjektive kognitive Einbußen erfragt:
- In welchen Leistungsbereichen treten sie auf und führen sie zu alltagspraktischen Konsequenzen? Der Patient sollte motiviert werden, exemplarische Beispiele aus dem Alltag zu benennen.)
- Gibt es Schwankungen in der Ausprägung der Defizite und Progredienz?
- Stehen Einbußen im zeitlichen Zusammenhang mit akuten Ereignissen (z.B. Schlaganfall, depressive Episode)? Sind mehrere kognitive Domänen berührt, traten die Defizite zeitgleich oder nacheinander auf? Was war das erste bemerkte Symptom?
- Sorgen hinsichtlich der Entwicklung einer Demenzerkrankung, die Motivation zur Diagnostik (eigen-/fremdmotiviert, auch „Rentenbegehren“) oder begleitende depressive Symptome sind klinisch bedeutsame Parameter, die auf unterschiedliche Ätiologie der subjektiven kognitiven Defizite hinweisen können und daher exploriert werden sollten [3].
- Ein individuelles Risikoprofil für kognitive Einbußen sollte über die Anamnese erstellt werden. Neben prädisponierenden Variablen sollten auch protektive Faktoren erhoben werden, die illustrieren, ob oder wie ein Patient bereits aktiv versucht, seine kognitive Leistungsfähigkeit zu stabilisieren (z.B. körperliche Aktivität, kognitive Anregung im Alltag oder über gezieltes „Training“).
- Eine Fremdanamnese kann wichtige klinischen Zusatzinformationen liefern: Sind die Einbußen nur für nahe Angehörige oder überhaupt für Außenstehende greifbar? Gibt es eine Diskrepanz in der subjektiven Wahrnehmung des Betroffenen und der externen Perspektive? Sind Alltagskompetenzen beeinträchtigt und Unterstützung erforderlich? Ist der Patient verunsicherbar, zeigt er vermehrtes Rückversicherungsverhalten und haben sich neben kognitiven Leistungen auch Wesenszüge verändert? Sind Verhaltensbesonderheiten aufgetreten?
Körperliche Untersuchung
- Eine körperliche Untersuchung sollte orientierend und individuell symptomorientiert vertiefend durchgeführt werden. Sie kann indirekt Hinweis auf Erkrankungen mit potenziell dyskognitiven Begleiterscheinungen geben (z.B. Leberzirrhose bei hepatischer Enzephalopathie, Struma bei Hypothyreose).
- In der neurologischen Untersuchung sind insbesondere Bewegungsstörungen (Parkinson-Syndrom, Ataxie), Sprach- und Sprechstörungen, Okulomotorikstörungen und auch Frontalhirnzeichen Beispiele für zahlreiche Pathologien, durch die ein Hinweis auf die Ätiologie kognitiver Einbußen gewonnen werden kann.
Labor
- Die laborchemische Diagnostik sollte Parameter mit bekanntem Bezug zu dyskognitiven Effekten einbeziehen. Hypothyreose, Hyponatriämie und Vitamin-B12-Mangel sind hierfür Beispiele. Eine Anämie oder stark schwankende Blutzuckerwerte können ebenfalls kognitive Leistungen beeinträchtigen, daher sollten entsprechende Parameter Teil der Diagnostik sein, ebenso Untersuchungen zur Leber- und Nierenfunktion.
- Liquordiagnostik (Neurodegenerationsparameter: verschiedene β-Amyloid- und Protein-Tau-Spezies) sollte nur erfolgen, wenn ein Effekt des Ergebnisses auf das klinische Management zu erwarten ist („timely diagnosis“), z. B. bei grenzkompensiertem MCI oder vor evtl. Anti-Amyloid-Antikörpertherapie [2], insbesondere eine präklinische Alzheimer-Erkrankung ist zu berücksichtigen. Liquorbefunde sind ohne klinisches Syndrom nicht hinreichend aussagekräftig und können falsch positiv oder falsch negativ sein.
Mikrobiologie
-
Lues- und HIV-Infektionen sollten bei klinischem Verdacht ausgeschlossen werden.
Bildgebende Diagnostik
PET
- Mittels Positronenemissionstomografie (PET) kann der Glukosestoffwechsel indirekt über regionale zerebrale Funktionsstörungen Aufschluss geben, ein Amyloid-PET (3 verschiedene Amyloid-Tracer in EU zugelassen) stellt die Verteilung von Amyloidplaques dar. Beide Verfahren können in der Differenzialdiagnostik neurodegenerativer Erkrankungen hilfreich sein, weniger bei der Verlaufskontrolle von kognitiven Einbußen. Das Amyloid-PET sollte nur erfolgen, wenn die MCI-Ätiologie nach klinischer, neuropsychologischer, bildgebender und liquordiagnostischer Untersuchung unklar verbleibt [2]
- Das Vorliegen eines MCI kann heute noch nicht mit Hilfe von Biomarkern bewiesen werden, es ist ein klinisch und testpsychometrisch definiertes Syndrom.
MRT
-
Eine MRT-Bildgebung des Gehirns ist Standard. Neben dem Ausschluss seltener Ursachen wie Hirntumoren können z. B. vaskuläre Veränderungen damit gut beurteilt werden. Auf eine CT sollte nur bei MRT-Kontraindikationen, ausgeprägter Klaustrophobie oder bei speziellen Fragestellungen ausgewichen werden. Unter positivdiagnostischem Aspekt bietet die MRT auch die Möglichkeit, regionale Atrophiezeichen zu erkennen. Automatisierte, volumetrische Analyseverfahren können in Ergänzung zur visuellen neuroradiologischen Befundung eingesetzt werden [2].
Instrumentelle Diagnostik
Neuropsychologische (testpsychometrische) Diagnostik
- Kurztestverfahren (Screeningtests; z.B. Minimental-Status-Test, MoCA, DemTect, Uhrentest) sind allein nicht ausreichend. Insbesondere bei leichten kognitiven Beeinträchtigungen sind sie zu einfach („Ceiling-Effekt“) und einzelne kognitive Domänen können nur unzureichend beurteilt werden, wobei der MoCA im Gegensatz zu anderen kognitiven Assessments eine höhere Sensitivität zur MCI-Detektion besitzt (cut-off 25/30 Punkten) [8].
- Eine differenzierende leistungspsychologische Untersuchung ist Standard. Die Testbatterie sollte mindestens folgende Testverfahren einschließen:
- Intelligenztest (Screening), z.B. MWT-B
- globale Kognition (Screening), z.B. MMST oder MoCA
- verbales und visuelles Gedächtnis: z.B. CERAD
- Merkspanne/Arbeitsgedächtnis: z.B. NAI
- visuell-konstruktive Leistungen, z.B. CERAD
- Wortfindung, Wortflüssigkeit, z.B. Boston Naming Test, Tiere-Test
- Aufmerksamkeit, Konzentration: z.B. TMT A/B, NAI, Labyrinth-Test, Farb-Wort-Test
- Neuropsychologische Diagnostik muss im klinischen Kontext beurteilt werden. Die Vereinbarkeit klinischer und testpsychometrischer Befunde sollte beurteilt werden. Aggravation, Simulation oder funktionelle kognitive Störungen können vorkommen, ein deutliches Defizitprofil in der formalen Testung muss im klinischen Eindruck und auch im Alltagskontext eine Entsprechung finden.
EEG
-
EEG-Veränderungen sind im Rahmen einer leichten kognitiven Störung entweder nicht vorhanden oder unspezifisch. Ein EEG sollte aber erfolgen, wenn bei episodisch auftretenden Defiziten klinisch der Verdacht auf eine transiente epileptische Aktivität (TEA) besteht.
Histologie, Zytologie und klinische Pathologie
Molekulargenetische Diagnostik
- Sie ist angezeigt bei V.a. familiäre neurodegenerative Syndrome, z.B. durch Mutationen im Amyloid-Precursor-Gen oder den Präsenelin-1- und -2-Genen.
- Eine ApoE-Genotypisierung soll unter diagnostischen Gesichtspunkten gemäß aktueller Empfehlungen nicht erfolgen, ist aber vor Anti-Amyloid-Antikörpertherapie obligatorisch [2]
- Bei der Erwägung molekulargenetischer Untersuchungen ist das Gendiagnostikgesetz zu beachten.
Differenzialdiagnosen
-
Die primären Symptome sind unspezifisch, sodass alle unklaren, fieberhaften Erkrankungen in Betracht gezogen werden sollten. Ebenfalls sind in Abhängigkeit von weiteren Symptomen (z.B. gastroenteraler Manifestation) weitere differenzialdiagnostische Erkrankungen in Erwägung zu ziehen.
-
Wichtige Differenzialdiagnosen von unklaren fieberhaften Erkrankungen: Amöbenruhr, Arbovirusinfektionen, Bartonellose (Katzenkrankheit), Brucellose, Dengue-Fieber, Enzephalitiden verschiedener Ätiologie, grippale Infekte, HIV-Infektion,Kala-Azar (viszerale Leishmaniose), Rickettsiosen, Sinusitis, Typhus abdominalis, verschiedene Erreger einer Hepatitis, verschiedene Erreger von Enteritiden, verschiedene Erreger einer Meningitis.
Therapie
Therapeutisches Vorgehen
Spezifische, verlaufsmodulierende Medikamente zur Behandlung des MCI sind bislang ausschließlich für das MCI im Rahmen einer beginnenden Alzheimer-Krankheit (bei eindeutigem Biomarkernachweis) verfügbar (seit 2025 Lecanemab und Donaneab zugelassen). Für die off-label-Behandlung des MCI mit Acetylcholinesteraseinhibitoren besteht keine Evidenz [2]
- es bestehen hohe Anforderungen an die Indikationsprüfung vor Therapiebeginn und an das Therapiemonitoring unter laufender Anti-Amyloid-Antikörpertherapie (Kontraindikationen: Blutungsstörungen, orale Antikoagulation, ApoE-e4-Homozygotie, zerebrale Amyloidangiopathie, Z. n. intrazerebraler Blutung, schwere zerebrale Mikroangiopathie, schlecht eingestellter Hypertonus, Kontraindikationen gegen cMRT)
- Die kardiovaskulären Risikofaktoren werden behandelt.
- Die symptomatischen Ursachen für potenziell reversible kognitive Störungen (beispielsweise bei Depression, Hypothyreose oder Schlafstörungen) werden behandelt.
- Wichtig sind eine regelmäßige körperliche Aktivität und Förderung der kognitiven Reserve. Spezifische Formen kognitiven Leistungstrainings (bspw. Ergotherapie), auch am PC, ersetzen soziale Interaktionen nicht, können aber zusätzlich zur Stabilisierung beitragen.
- Dyskognitive Medikamente absetzen.
Nachsorge
- Klinische und testpsychometrische Reevaluationen sind sinnvoll. Das Intervall beträgt typischerweise zwischen 6 und 24 Monaten in Abhängigkeit von bisherigem klinischem Verlauf und vermuteter Ätiologie. Ein typisches Kontrollintervall bei einem amnestischen MCI sind 12 Monate.
- Bei Progredienz und Demenzverdacht sollte gegebenenfalls eine Biomarker-basierte Diagnostik ergänzt werden (Liquordiagnostik und/oder PET).
Verlauf und Prognose
- Die kognitiven Defizite im Rahmen eines MCI können prinzipiell remittieren, stabil bleiben oder progredient sein [1], [5]. Während Remissionen von objektivierbaren Einbußen eine primär neurodegenerative Genese nicht nahelegen und beispielsweise bei metabolischen Erkrankungen oder im Rahmen depressiver Syndrome auftreten können, finden sich stabile oder passager verbesserbare Ausprägungen häufig im Zusammenhang mit zerebrovaskulären Schädigungen.
- Eine primär amnestische leichte kognitive Störung zeigt mit 10–15% das höchste Risiko der Konversion zu einer Demenz vom Alzheimer-Typ [5].
Prävention
-
Die Behandlung kardiovaskulärer Risikofaktoren, eine gesunde Lebensweise mit regelmäßiger körperlicher und geistiger Aktivität sind Grundlagen der Primärprävention.
Synonyme
- leichte kognitive Einbuße
- leichte kognitive Störung
Keywords
- mild cognitive impairment (MCI)
- leichte kognitive Störung
- Prodromalstadium einer Demenz
- mild neurocognitive disorder
- minor neurocognitive disorder
Literatur
Quellenangaben
-
[1] Albert MS, DeKosky ST, Dickson D et al. The diagnosis of mild cognitive impairment due to Alzheimer’s disease: recommendations from the National Institute on Aging-Alzheimer’s Association workgroups on diagnostic guidelines for Alzheimer’s disease. Alzheimers Dement 2011; 7: 270–279
Suche in: PubMed Google Scholar -
[2] Deutsche Gesellschaft für Psychiatrie und Psychotherapie, Psychosomatik und Nervenheilkunde e.V. (DGPPN), Deutsche Gesellschaft für Neurologie e.V. (DGN). S3-Leitlinie Demenzen – Living Guideline. Version 5.2 (2025). AWMF-Registernummer: 038-013. Im Internet: https://register.awmf.org/de/leitlinien/detail/038-013.
-
[3] Haussmann R, Mayer-Pelinski R, Borchardt M et al. Extrinsic and Intrinsic Help-Seeking Motivation in the Assessment of Cognitive Decline. Am J Alzheimers Dis Other Demen 2018; 33: 215–220
Suche in: PubMed Google Scholar -
[4] Petersen C, Lopez O. Practice update summary: Mild cognitive impairment: Report of the Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of Neurology. Neurology 2018; 90: 126
Suche in: PubMed Google Scholar -
[5] Petersen RC, Negash S. Mild Cognitive Impairment: An Overview. CNS Spectr 2008; 13: 45–53
Suche in: PubMed Google Scholar -
[6] Robert RO, Becker JT et al. The incidence of mild cognitive impairment in the Pittsburgh Cardivascular Health Study-Cognition Study. Neurology 2012; 79: 1599
Suche in: PubMed Google Scholar -
[7] Rao V et al. (2022). Chemobrain: A review on mechanistic insight, targets and treatments. Adv Cancer Res. 155: 29-76.
Suche in: PubMed Google Scholar -
[8] Sun J, Dong Qu, Wang S-W et al. Artificial intelligence in psychiatry research, diagnosis, and therapy. Asian Journal of Psychiatry 2023; 87: 103609.
Suche in: PubMed Google Scholar -
[9] Van Dyck CH et al. (2023). Lecanemab in Early Alzheimer`s Disease. NEJM. 388: 842-9-21.
Suche in: PubMed Google Scholar -
[10] Sims JR et al. (2023). Donanemab in Early Symptomatik Alzheimer Disease The Trailblazer-ALZ 2 RCT. JAMA. 330(6): 512-27.
Suche in: PubMed Google Scholar -
[11] van Dyck CH et al. Lecanemab in Early Alzheimer’s Disease. N Engl J Med. 2023;388(1):9-21. doi: 10.1056/NEJMoa2212948.
Suche in: PubMed Google Scholar -
[12] Sims JR et al. Donanemab in Early Symptomatic Alzheimer Disease: The TRAILBLAZER-ALZ 2 Randomized Clinical Trial. JAMA. 2023;330(6):512-527. doi: 10.1001/jama.2023.13239.
Suche in: PubMed Google Scholar -
[13] Aisen PS et al. Clinical Core of the Alzheimer’s Disease Neuroimaging Initiative: progress and plans. Alzheimers Dement. 2010;6(3):239-46. doi: 10.1016/j.jalz.2010.03.006.
Suche in: PubMed Google Scholar